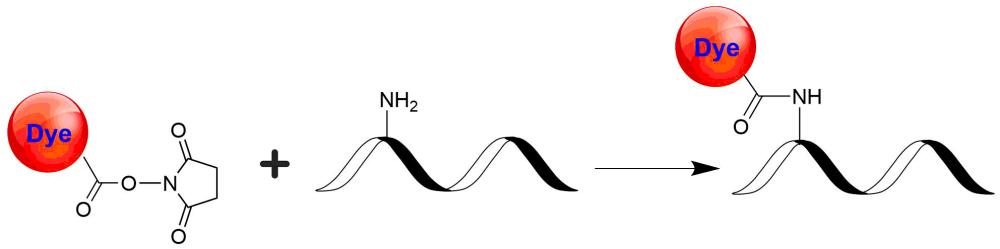
zFluor 647 琥珀酰亚胺酯
 |
货号 |
1500 |
存储条件 |
在零下15度以下保存, 避免光照 |
| 规格 |
1 mg |
价格 |
3264 |
| Ex (nm) |
648 |
Em (nm) |
668 |
| 分子量 |
853.04 |
溶剂 |
DMSO |
| 产品详细介绍 |
简要概述
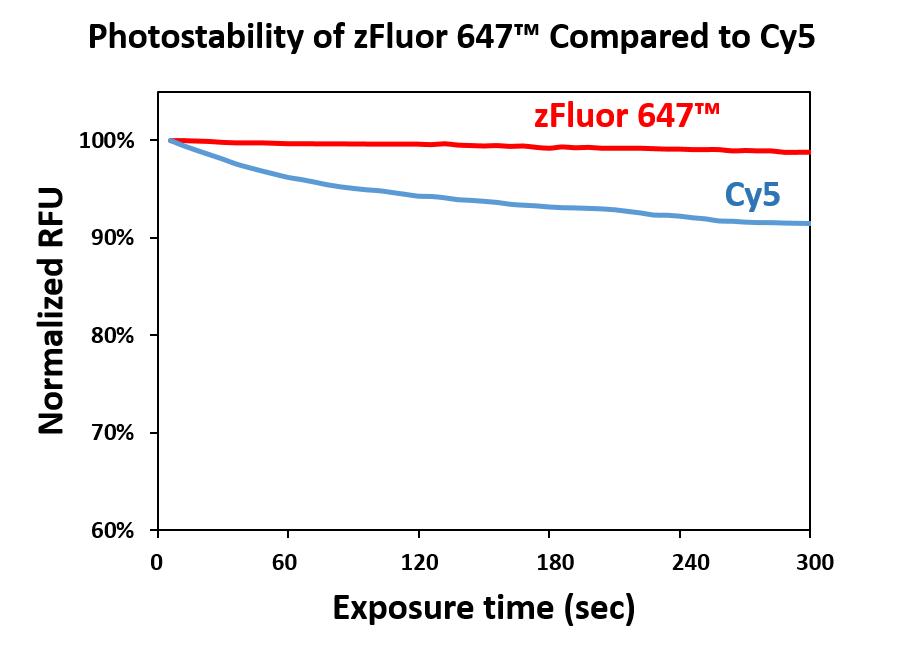
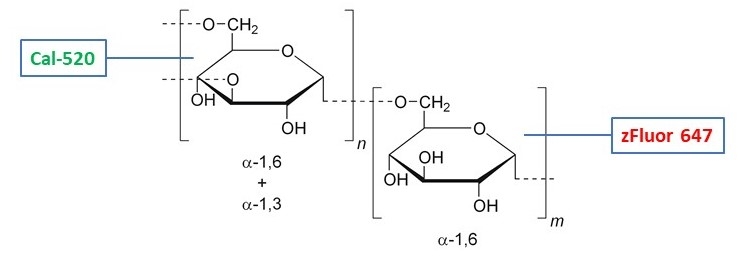
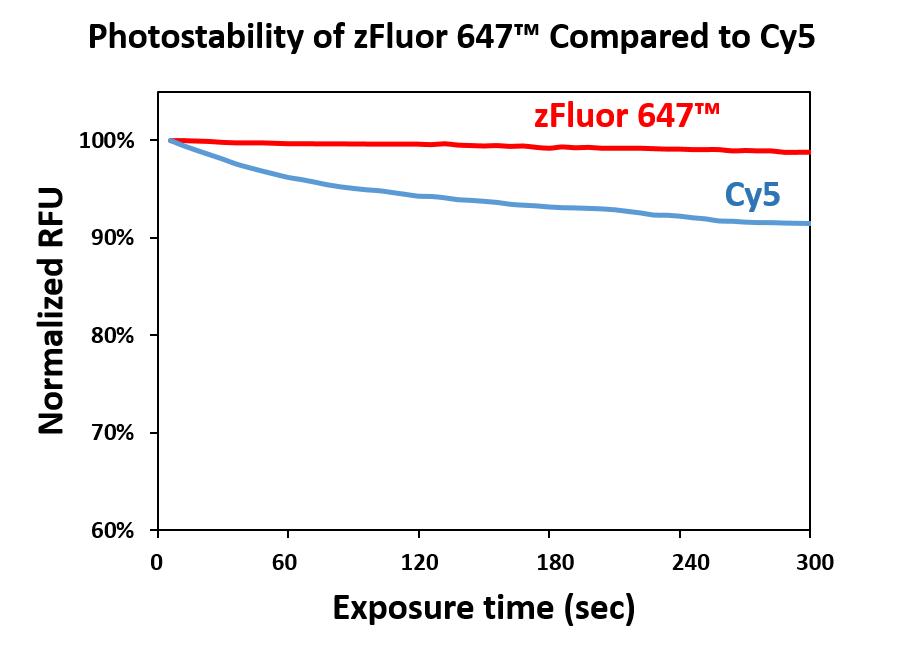
zFluor 647 琥珀酰亚胺酯是美国AAT Bioquest生产的荧光染料,与市场上其他类似波长染料相比,我们开发的zFluor 系列染料在给定波长下具有可能最高的光稳定性。zFluor 647具有与流行的Cy5®(GE Healthcare)和AlexaFluor®647(ThermoFisher)几乎相同的光谱特性。其高热和光稳定性使其成为单分子检测应用和高分辨率显微镜(如PALM,dSTORM和STED)的理想选择。在相同的测试条件下,zFluor 647具有比Cy5®和AlexaFluor®647高得多的臭氧稳定性,使其成为微阵列和其他生物芯片应用的更好选择。此外,zFluor 标记的寡核苷酸和多肽比AlexaFluor®647和Cy5®标记的更亮,更光稳。该特征对于荧光原位杂交(FISH)非常有用。它在633 nm的He-Ne激发光,氪的647 nm线处受到很好的激发。 -Ion激光器或发射650 nm的二极管激光器。金畔生物是AAT Bioquest的中国代理商,为您提供最优质的zFluor 647 琥珀酰亚胺酯。
点击查看光谱
点击查看实验方案
产品说明书
染色样本分析
操作步骤
1.准备蛋白质储备溶液(溶液A):
将100μL反应缓冲液(如1 M碳酸钠溶液或1 M磷酸盐缓冲液,pH~9.0)与900μL目标蛋白溶液(如抗体,蛋白质浓度> 2 mg / ml,如果可能)混合至100μL给予1 mL蛋白质标记原液。
注1:蛋白质溶液(溶液A)的pH值应为8.5±0.5。如果蛋白质溶液的pH低于8.0,则使用1M碳酸氢钠溶液或1M pH 9.0磷酸盐缓冲液将pH调节至8.0-9.0的范围。
注2:蛋白质应溶解于pH7.2-7.4的1X磷酸盐缓冲盐水(PBS)中。如果蛋白质溶解在Tris或甘氨酸缓冲液中,则必须用pH7.2-7.4的1X PBS透析,以除去广泛用于蛋白质沉淀的游离胺或铵盐(例如硫酸铵和乙酸铵)。
注3:用牛血清白蛋白(BSA)或明胶稳定的不纯抗体或抗体不能很好地标记。叠氮化钠或硫柳汞的存在也可能干扰缀合反应。可以通过透析或旋转柱除去叠氮化钠或硫柳汞,以获得极佳标记结果。
注4:如果蛋白质浓度低于2 mg / mL,则结合效率会显着降低。为获得极佳标记效率,建议极终蛋白质浓度范围为2-10 mg / mL。
2.准备染料储备溶液(溶液B):
将无水DMSO加入到iFluor 染料SE小瓶中以制备10-20mM储备溶液。 通过移液或涡旋混合均匀。
注意:在开始缀合前准备染料储备溶液(溶液B)。 及时使用。 染料储备溶液的长期储存可降低染料活性。 溶液B可在冰箱中保存两周,避光保存。 避免冻融循环。
3.确定极佳染料/蛋白质比例(可选):
注意:每种蛋白质都需要不同的染料/蛋白质比例,这也取决于染料的性质。蛋白质的过度标记可能不利地影响其结合亲和力,而低染料/蛋白质比率的蛋白质缀合物会降低灵敏度。我们建议您通过使用连续不同量的标记染料溶液重复步骤4和5来实验确定极佳染料/蛋白质比率。通常,对于大多数染料 – 蛋白质缀合物,推荐使用4-6种染料/蛋白质。
3.1使用10:1摩尔比的溶液B(染料)/溶液A(蛋白质)作为起始点:将5μl染料储备溶液(溶液B,假设染料储备溶液为10 mM)加入到样品瓶中。蛋白质溶液(95μl溶液A)有效摇动。假设蛋白质浓度为10mg / mL并且蛋白质的分子量为~200KD,蛋白质的浓度为~0.05mM。
注意:蛋白质溶液中DMSO的浓度应<10%。
3.2运行缀合反应(参见下面的步骤4)。
3.3重复#3.2,溶液B /溶液A的摩尔比为5:1;分别为15:1和20:1。
3.4使用预制的旋转柱纯化所需的缀合物。
3.5计算上述4种结合物的染料/蛋白质比(DOS)(见说明书)。
3.6运行上述4种结合物的功能测试,确定极佳的染料/蛋白质比例,以扩大标记反应。
4.运行结合反应:
4.1有效加入适量的染料储备溶液(溶液B)到蛋白质溶液(溶液A)的小瓶中晃动。
注意:溶液B /溶液的极佳摩尔比由步骤3.6确定。如果跳过步骤3,我们建议使用10:1溶液B(染料)/溶液A(蛋白质)的摩尔比。
4.2继续在室温下旋转或摇动反应混合物30-60分钟。
5.纯化缀合物
以下方案是使用Sephadex G-25柱纯化染料 – 蛋白质缀合物的实例。
5.1按照制造说明准备Sephadex G-25色谱柱。
5.2将反应混合物(直接从步骤4)加载到Sephadex G-25柱的顶部。
5.3样品在顶部树脂表面下方运行时立即加入PBS(pH 7.2-7.4)。
5.4向所需样品中加入更多PBS(pH 7.2-7.4)以完成色谱柱纯化。 合并含有所需染料 – 蛋白质缀合物的级分。
注1:立即使用时,染料 – 蛋白质偶联物需要用染色缓冲液稀释,并等分多次使用。
注2:对于长期储存,染料 – 蛋白质缀合物溶液需要浓缩或冷冻干燥
参考文献
Capillary-Driven Microfluidic Chips for Miniaturized Immunoassays: Patterning Capture Antibodies Using Microcontact Printing and Dry-Film Resists
Authors: Temiz, Y.; Lovchik, R. D.; Delamarche, E.
Journal: Methods Mol Biol (2017): 37-47
Generation and Characterization of Virus-Enhancing Peptide Nanofibrils Functionalized with Fluorescent Labels
Authors: Rode, S.; Hayn, M.; Rocker, A.; Sieste, S.; Lamla, M.; Markx, D.; Meier, C.; Kirchhoff, F.; Walther, P.; Fandrich, M.; Weil, T.; Munch, J.
Journal: Bioconjug Chem (2017): 1260-1270
Single nucleotide polymorphism discrimination with and without an ethidium bromide intercalator
Authors: Fenati, R. A.; Connolly, A. R.; Ellis, A. V.
Journal: Anal Chim Acta (2017): 121-128
Background Suppression in Imaging Gold Nanorods through Detection of Anti-Stokes Emission
Authors: Carattino, A.; Keizer, V. I.; Schaaf, M. J.; Orrit, M.
Journal: Biophys J (2016): 2492-2499
Absolute two-photon excitation spectra of red and far-red fluorescent probes
Authors: Velasco, M. G.; Allgeyer, E. S.; Yuan, P.; Grutzendler, J.; Bewersdorf, J.
Journal: Opt Lett (2015): 4915-8
Diffusion coefficients and dissociation constants of enhanced green fluorescent protein binding to free standing membranes
Authors: Thomas, F. A.; Visco, I.; Petrasek, Z.; Heinemann, F.; Schwille, P.
Journal: Data Brief (2015): 537-41
Resonant Scanning with Large Field of View Reduces Photobleaching and Enhances Fluorescence Yield in STED Microscopy
Authors: Wu, Y.; Wu, X.; Lu, R.; Zhang, J.; Toro, L.; Stefani, E.
Journal: Sci Rep (2015): 14766
Synthesis and characterization of fluorescence-labelled silica core-shell and noble metal-decorated ceria nanoparticles
Authors: Herrmann, R.; Rennhak, M.; Reller, A.
Journal: Beilstein J Nanotechnol (2014): 2413-23
The contribution of reactive oxygen species to the photobleaching of organic fluorophores
Authors: Zheng, Q.; Jockusch, S.; Zhou, Z.; Blanchard, S. C.
Journal: Photochem Photobiol (2014): 448-454
Topical drug delivery to retinal pigment epithelium with microfluidizer produced small liposomes
Authors: Lajunen, T.; Hisazumi, K.; Kanazawa, T.; Okada, H.; Seta, Y.; Yliperttula, M.; Urtti, A.; Takashima, Y.
Journal: Eur J Pharm Sci (2014): 23-32
相关产品
| 产品名称 |
货号 |
| iFluor 647琥珀酰亚胺酯 |
Cat#1031 |
| zFluor 633 琥珀酰亚胺酯 |
Cat#1510 |
说明书
zFluor 647 琥珀酰亚胺酯.pdf